Koronaviruksen näytteiden testauksen tehostaminen onnistuu yksilöiden näytteiden yhdistämisellä
Koronaviruksen (SARS-CoV-2/COVID-19) aiheuttama pandemia on aiheuttanut kuormitusta koronanäytteiden testaukselle, johon on yritetty etsiä helpotusta, muun muassa massatestauksella [1]. Populaatioiden tarkka seuranta ja seulonta ovat tärkeitä keinoja estää viruksen leviämistä. Jotta useita näytteitä voitaisiin käsitellä tämän toteuttamiseksi, testikapasiteetin lisäämiseen on ehdotettu uusia keinoja.
Koronaviruksen testaaminen tehdään yleisesti tunnistamalla sen RNA-genomi käyttämällä polymeraasiketjureaktio (PCR) -menetelmää [2]. PCR-menetelmä on tarkka keino havaita positiiviset näytteet, mutta menetelmän käyttöä rajoittaa vaaditut reagenssit, PCR-laitteen käyttöön vaadittu aika, työajat ja logistiikka [3]. Jokaisen yksilön erillinen testaus on siis kallista ja hidasta. Testikapasiteetin määrää pyritään lisäämään hyödyntämällä massatestauksia. Massatestauksen tarkoituksena on pystyä testaamaan usean yksilön näytteet laittamalla ne yhteen. Usean yksilön näytteet voidaan testata yhdellä kertaa sekä säilöä mahdollisia jatkotutkimuksia varten.
Massatestauksessa käytetään niin sanottua kaksivaiheista menetelmää [4]. Siinä merkitään ihmisten määrä yhdessä ryhmässä. Tutkittavien henkilöiden näytteet jaetaan kahteen osaan, jossa toinen osa sekoitetaan kaikkien ryhmän yksilöiden kesken, ja toinen osa näytettä pidetään tallessa myöhempää käyttöä varten. Jos ryhmän näytteen tulos on negatiivinen, kaikki yksilöt oletetaan negatiivisiksi. Jos näyte on positiivinen, vähintään yksi henkilö on positiivinen. Jokainen yksilö positiivisessa näyteryhmässä testataan uudestaan säilötetyistä näytteistä.
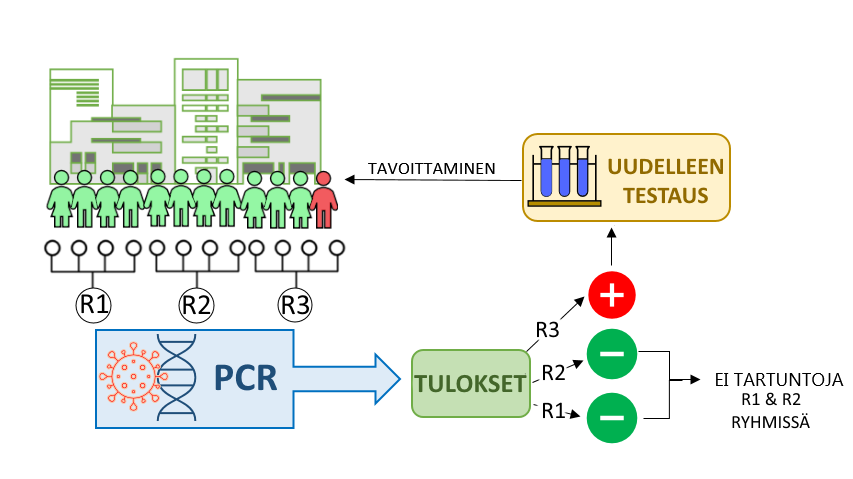
- Massatestauksella voidaan vähentää tarvittavien testien määrää yhdistämällä näytteitä. Positiivisen ryhmän tulos käsitellään uudestaan testaamalla jokaisen yksilön näyte erikseen.
Miten ryhmän koko valitaan, jotta tulokset ovat riittävän tarkkoja, mutta samalla tehostavat prosessia vähentämällä tarvittavien testien määrää? Valintaan voidaan soveltaa Robert Dorfmanin vuonna 1943 kehittämää laskentamenetelmää, jossa mallinnettiin todennäköisyyttä havaita infektoitunut yksilö ryhmästä [5]. Kyseisessä mallissa ryhmäkoon määrittäminen on hyvin riippuvainen esiintymisasteesta. Esiintymisaste on epidemiologiassa käytetty mitta, joka kertoo tapausten määrän annetussa tilastollisessa populaatiossa tiettynä ajanjaksona, jaettuna yksilöiden määrällä annetussa populaatiossa [4]. Esiintyvyysasteeseen sisällytetään määritellyn ajanjakson kaikki uudet sekä ennestään olevat tapaukset populaatiossa. Koronaviruksen tapauksessa tutkimukset ovat suosineet viiden yksilön ryhmiä, jotta testit ovat riittävän tarkkoja, mutta myös vähentävät riittävästi vaadittavien testausten määriä [6], [7], [8].
On kuitenkin otettava huomioon, että esiintymisasteen kasvaessa, eli koronavirustapausten määrän noustessa, massatestauksen ryhmänkokoa on pienennettävä tai luovuttava siitä kokonaan [4], [9]. Jos ryhmäkoko pysyy suurena ja esiintymisaste on suuri, moni testattavista näytteistä olisi positiivisia ja aiheuttaisi testien uusimista. Tämä olisi tehotonta. Esiintymisasteen ollessa pieni, ryhmäkokoa voidaan kasvattaa, sillä positiivisia näytteitä tulisi seurannassa vähemmän, jolloin kokonaistestien määrä saadaan huomattavasti pienemmäksi.
Massatestausta voitaisiin hyödyntää esimerkiksi palvelu- tai oppilaitosten seurannassa. Jos ajatellaan vaikka, että oppilaitoksessa on yhteensä 300 oppilasta, jokaisen yksilöllinen testaus vaatisi normaalisti 300 testiä. Jos oppilaat jaetaan esimerkiksi viiden hengen joukkoihin, saadaan yhteensä 60 ryhmää. Jos oletetaan esimerkiksi 5 %:n esiintyvyysaste, 300 oppilaasta on infektoitunut 15 oppilasta. Jos jokainen infektoitunut on eri ryhmässä, joudutaan 60:n testin lisäksi tekemään 75 yksilöllistä testiä positiivisissa ryhmissä oleville henkilöille. Yhteensä testejä tällä menetelmällä tulisi 135, mikä olisi silti 55 % vähemmän kuin kaikkien yksilöiden testaaminen. Tehokkuus ja rahallinen säästö kuitenkin vähenee esiintymisasteen kasvaessa. Esimerkiksi esiintyvyysasteen ollessa 15 %, testien määrä nousee edellisessä esimerkissä 285:een.
Näytteiden ryhmittämisellä on myös negatiiviset puolensa, jotka liittyvät testin tuottamiin mahdollisiin virheisiin. Jos unohdetaan ihmisen tekemät virheet, väärät tulokset liittyvät lähinnä testin herkkyyteen ja spesifisyyteen [3]. Jos usean yksilön näyte sekoitetaan yhteen, se aiheuttaa yksilön näytemateriaalin laimentumista. Mitä isompaa ryhmää käytetään, sitä suuremmaksi laimentuminen kasvaa ja niin sanottu tyyppi II virheen marginaali nousee. Tämä tarkoittaa sitä, että saadaan negatiivinen tulos, vaikka joukossa olisi positiivinen tapaus, toisin sanoen, testin sensitiivisyys heikkenee. Toisaalta massatestauksella vääriä positiivisia saadaan vähemmän, sillä kaksivaiheisessa menetelmässä positiiviset näytteet tutkitaan kahteen kertaan, eli spesifisyys paranee. Laimentumisen estämiseksi ryhmäkoko voidaan pitää suhteellisen pienenä. Tutkimuksissa on havaittu, että maksimissaan viiden yksilön ryhmässä laimentumisesta aiheutuvaa virhettä ei olla havaittu [6], [7], [8].
Tarkkuutta testeihin on myös ehdotettu mahdollisesti tarkemmalla menetelmällä, jossa myös negatiiviset näytteet varmennetaan uudella testauksella [10]. Jos uudessa testauksessa saadaankin positiivinen tulos, ryhmän näytteet jaetaan puoliksi kahteen eri ryhmään ja testataan uudestaan. Tämä positiivisten ryhmien jakaminen toistetaan niin monta kertaa kuin on tarpeen, jossa tarvittaessa päädytään testaamaan yksittäinen näyte uudelleen. Tämän menetelmän on havaittu tuottavan vähemmän vääriä negatiivisia ja vääriä positiivisia tuloksia [10], [11].
Kirjallisuus
[1] Centers for Disease Control and Prevention (CDC). Interim Guidance for Use of Pooling Procedures in SARS-CoV-2 Diagnostic, Screening, and Surveillance Testing. https://www.cdc.gov/coronavirus/2019-ncov/lab/pooling-procedures.html, viitattu 24.11.2020.
[2] Terveyden ja hyvinvoinnin laitois (THL). Koronaviruksen COVID-19 laboratoriotutkimukset. https://thl.fi/fi/web/infektiotaudit-ja-rokotukset/taudit-ja-torjunta/taudit-ja-taudinaiheuttajat-a-o/koronavirus-covid-19/koronaviruksen-covid-19-laboratoriotutkimukset, viitattu 25.11.2020.
[3] Bikovski A. & Bentele K. 2020. Pooling of coronavirus tests under unknown prevalence. Epidemiol Infect 148, e183, 1–4. doi: 10.1017/S0950268820001752
[4] Centers for Disease Control and Prevention (CDC). Principles of Epidemiology in Public Health Practice, 3rd An Introduction to Applied Epidemiology and Biostatistics. Measures of Risk P. 3–17.
[5] Dorfman R. Detection of Defective Members. Ann Math. Statist 14, No. 4, 436–440.
[6] Abdalhamid B., et al. 2020. Assessment of Specimen Pooling to Conserve SARS CoV-2 Testing Resources. Am J Clin Pathol, Vol. 153, Iss. 6, P. 715–718.
[7] Hogan A.C., et al. 2020. Sample Pooling as a Strategy to Detect Community Transmission of SARS-CoV-2. JAMA. 323(19):1967–1969. doi:10.1001/jama.2020.5445.
[8] Schmidt M., et al. 2020. FACT- Frankfurt adjusted COVID-19 testing- a novel method enables high-throughput SARS-CoV-2 screening without loss of sensitivity. MedRxiv. doi:1101/2020.04.28.20074187.
[9] 2020. Pooling of asymptomatic SARS COV-2 COVID-19 samples for (PCR/or other) testing. Guidance. https://www.england.nhs.uk/coronavirus/wp-content/uploads/sites/52/2020/09/C0777-sample-pooling-sop-v1.pdf, viitattu 25.11.2020.
[10] Litvak E., et al. 2020. The Right Kind of Pooled Testing for the Novel Coronavirus: First, Do No Harm. AJPH.
[11] Litvak E., et al. 1991. Screening for the Presence of a Disease by Pooling Sera Samples. J Am Stat Assoc. 89, Iss. 426.







